 La termometría se encarga de la Medición de la Temperatura de cuerpos o Sistemas. Para this aleta, se utilizació el termómetro, Que Es Un Instrumento Que se basa en el Cambio de Alguna Propiedad de la materia DEBIDO al efecto del calor; Así se Tiene el termómetro de mercurio y de alcohol, Que se Basan en la dilatación, los termopares Que Deben Do FUNCIONAMIENTO Al Cambio de la conductividad eléctrica, los ópticos Que detectan la variation de la Intensidad del rayo EMITIDO Cuando Se Refleja En un Cuerpo caliente .
La termometría se encarga de la Medición de la Temperatura de cuerpos o Sistemas. Para this aleta, se utilizació el termómetro, Que Es Un Instrumento Que se basa en el Cambio de Alguna Propiedad de la materia DEBIDO al efecto del calor; Así se Tiene el termómetro de mercurio y de alcohol, Que se Basan en la dilatación, los termopares Que Deben Do FUNCIONAMIENTO Al Cambio de la conductividad eléctrica, los ópticos Que detectan la variation de la Intensidad del rayo EMITIDO Cuando Se Refleja En un Cuerpo caliente .
EXISTEN Varias escalas termométricas párrafo Medir Temperaturas, relativas Y absolutas. A partir de La Sensación fisiológica, Es Posible Hacerse Una idea aproximada de la Temperatura de La que se ENCUENTRA Objeto ONU. Pero ESA apreciación directa this por limitada Diferentes Factores; Así el Intervalo de Temperaturas A lo largo del cual sea Esto Es Posible es pequeño; : Además, párr Una Misma Temperatura La Sensación Correspondiente PUEDE Variar SEGUN SE Haya estado previamente en contacto con Otros cuerpos Más calientes o mas Fríos y, poco por Si Fuera, no es Posible expresar con precisión en forma de quantity los Resultados de Este tipo de apreciaciones subjetivas. : Por ello párrafo Medir Temperaturas se recurre a los Termómetros. En TODO Cuerpo material de la Variación de la Temperatura va Acompañada de la Correspondiente Variación de Otras propiedades medibles, de Modo Que A Cada valor de Aquella le corresponde Solo Un valor de this. Tal es el Caso de la Longitud De Una varilla metálica, de la Resistencia Eléctrica de metal de la ONU, de la Presión de gas de la ONU, del volumen de Líquido un, etc. Estas magnitudes Cuya variation this Ligada a la de la Temperatura se denominan propiedades termométricas , Porque pueden Ser las empleadas en la construcción de Termómetros. Para Definir Una escala de Temperaturas es Necesario Elegir Una Propiedad termométrica Que REUNA las Siguientes Condiciones: La Expresión matemática de la Relación Entre la propiedad y la Temperatura Dębe Ser Conocida.
La termométrica Propiedad Ser Dębe lo Bastante sensata una las con variaciones de Temperatura Como párr Poder Detectar, con Una precisión Que aceptable, pequeños Cambios térmicos. El Rango de Temperatura Dębe accesible grande Suficientemente ser. Una Vez Que la propiedad termométrica ha Sido Elegida, la elaboración De Una escala termométrica o de Temperaturas Lleva CONSIGO, al Menos, DOS Operaciones; Por Una parte, la determinacion de los puntos fijos o Temperaturas de Referencia Que permanecen Constantes en la naturaleza y, por otra, la división del Intervalo de Temperaturas Correspondiente unos cuentos puntos fijos en unidades o grados. Lo Que Se Necesita párrafo Construir termómetro un, fijos de Puntos de hijo, es Decir Procesos en los Cuales La Temperatura permanece constante. EJEMPLOS de Procesos of this tipo hijo El Proceso de ebullición y el Proceso de fusión.
Mediante la calorimetría Se Puede Medir el calor del una Reacción química o la ONU Cambio Físico Usando ONU calorímetro Llamado Instrumento. Pero también Se Puede emplear ONU Modo indirecto calculando el calor Que los Organismos vivos Producen un partir de la Producción de Dióxido de Carbono y de Nitrógeno (urea en Organismos terrestres), y del Consumo de oxígeno. Donde? U = Cambio de Energía interna Como la pressure ningún Se mantiene constante, el calor Medido sin repre el Cambio de entalpía. Calorimetría un pressure constante El calor Medido Es Igual Al Cambio en la Energía interna del Sistema Menos El Trabajo Realizado: Como la pressure Se mantiene constante, el calor Medido repre el Cambio de entalpía.
EL CALOR
Es El Proceso de Transferencia de Energía de Entre Diferentes cuerpos o Diferentes Zonas de ONU Mismo Cuerpo Que se encuentran una Distintas Temperaturas. Este Flujo siempre Ocurre desde el Cuerpo de alcalde Temperatura Hacia el Cuerpo de menor, temperatura, ocurriendo la Transferencia Hasta Que Ambos cuerpos se encuentren en equilibrio térmico (EJEMPLO: una bebida fría dejada en Una habitación se entibia). La Energía Puede Ser transferida por Diferentes Mecanismos, Entre Los Que Cabe reseñar la radiación, la Conducción y La convección, AUNQUE En La Mayoría de los Procesos reales Todos se encuentran Presentes en alcalde o menor grado.
Es La Sensación de calor o frío al tocar Una Sustancia Depende de su Temperatura, de la Capacidad de la Sustancia párrafo Conducir el calor y de Otros Factores.
En Física, se definirá Como una magnitud escalar Relacionada con la Energía Interna de termodinámico Sistema de Naciones Unidas, DEFINIDA POR EL Principio cero de la termodinámica. Más especificamente, this Relacionada Directamente con la parte de la Energía interna Conocida Como «Energía cinética», Que es la Energía Asociada a los Movimientos de las Partículas del Sistema, mar En un traslacional SENTIDO, rotacional, o en forma de Vibraciones. A Medida De que el alcalde de mar la Energía cinética de Sistema de las Naciones Unidas, se obser Que ESTE SE Encuentra Más «caliente»; es Decir, Mayor Que Do Temperatura es.
ESCALA DE LA TERMOMETRIA
En la Actualidad se Emplea Diferentes escalas Temperatura. Entre ellas TENEMOS:
ESCALA CELSIUS O CENTÍGRADA
Advertir Que las Temperaturas una cola se verificaban cuentos Cambios de estado era de las Constantes a la Presión atmosférica. Asignó al Primero el valor 0 y al Segundo el valor 100, con lo cual sea fijo el valor del grado Celsius (° C) Como la centésima parte del Intervalo de Temperatura comprendido Entre OEN dos puntos fijos. Para escala this, Estós Valores se Escriben Como 100 ° C y 0 ° C y se leen a 100 grados centígrados y 0 grados centígrados, respectivamente.
ESCALA FAHRENHEIT
Grado Fahrenheit. En los Países anglosajones se pueden Encontrar AÚN Termómetros Graduados en grado Fahrenheit (° F), por Propuesta Gabriel Fahrenheit en 1724. La escala Fahrenheit difiere de la Celsius del tanto en los Valores ASIGNADOS a los Puntos de Encuentro fijos, Como En El Tamaño de los grados. Son en la escala Fahrenheit los puntos fijos los de ebullición y fusión De Una Disolución de cloruro amónico en agua. Así al punto imprimación fijo se le atribuye el valor 32 y al Segundo el valor 212. Para Pasar De Una a otra escala es Preciso emplear la Ecuación: t (° F) = (9/5) * t (° C) + 32 ot (° C) = (5/9) * [t (° F) - 32] t Donde (° F) repre La Temperatura expresada en grados Fahrenheit yt (° C) la expresada en grados Celsius. Su utilizacion se circunscribe a los Países anglosajones ya Japón, AUNQUE Existe Una Marcada Tendencia a la unificación de Sistemas en la escala Celsius.
ESCALA KELVIN O ABSOLUTA
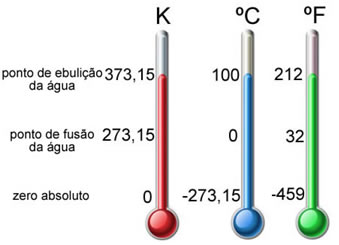
Se Comparan las escalas Celsius y Kelvin Mostrando los Puntos de Referencia Anteriores a 1954 y los posteriores párr Mostrar CÓMO Ambas Convenciones coinciden. De negro de color Aparecen El Punto de triple del agua (0,01 ° C, 273,16 K) y cero absoluto el (-273,15 ° C, 0 K). De gris color de los Puntos de congelamiento (0,00 ° C, 273,15 K) y ebullición del agua (100 ° C, 373,15 K). Si bien en la vida Diaria las escalas Celsius y Fahrenheit hijo las mas Importantes, en Ámbito Científico se EE.UU. otra, Llamada "absoluta" o Kelvin, en honor a un señor Lord Kelvin.
La Relación Con La escala Celsius Viene dada por la Ecuación: T (K) = t (° C) + 273,15 ot (° C) = T (K) - 273,15 T (K) = (5/9) * [t (° F) + 459,67] ot (° F) = (5/9) * T (K) - 459,67 Siendo T (K) La Temperatura expresada en kelvin.